日機装、日本ベーリンガーインゲルハイム、金沢大学が共同研究 動物実験に代わり細胞実験で再現できる創薬研究用ヒト腎細胞の開発に成功 ~研究成果がDrug Metabolism and Dispositionに掲載~
報道関係者向け情報
このホームページでは、国内の報道関係者の方々を対象に、ベーリンガーインゲルハイムジャパングループ各社の情報ならびに関連情報をご提供しています。一般の方に対する情報提供を目的としたものではありませんのでご了承ください。
日機装株式会社、日本ベーリンガーインゲルハイム株式会社および金沢大学医薬保健研究域薬学系の玉井郁巳教授らの研究グループは、世界で初めて、通常の培養条件では観察できなかった腎臓の機能を有した、創薬研究用ヒト腎細胞『3D-RPTEC』の開発に成功しました。今回開発した技術は、創薬研究において、主に動物実験で行っていた薬物の評価を細胞実験に代替できること、また創薬プロセスの効率化に貢献することが期待されます。
本研究成果は、2023年6月29日科学誌『Drug Metabolism and Disposition』(https://dmd.aspetjournals.org/content/early/2023/06/29/dmd.122.001171)に掲載されました。

■世界初、創薬研究用ヒト腎細胞『3D-RPTEC』とは
創薬研究用ヒト腎細胞とは、市販されているヒト腎由来細胞を特殊な培養方法で培養することにより、これまで観察することが困難であった腎臓の機能を再現した世界で初めてのヒト腎細胞です。実際に主要な薬物トランスポーター※20種ほどが機能することが確認されています。
※薬物トランスポーター:細胞膜に存在するタンパク質。医薬品を含む内因性/外因性低分子物質を細胞内に取り込む、あるいは細胞外へ排出させる装置の役割を持っている。腎細胞には、薬物輸送に関わる多数のトランスポーターの存在が知られている。
■創薬研究用ヒト腎細胞開発の背景
創薬研究において、薬物の評価(薬物動態や毒性)には主に動物実験が行われていますが、種差の問題や動物愛護の観点から、近年、動物実験の代わりに細胞実験によって「試験管内(=in vitro)」で再現し評価することが求められています。動物ではなく、ヒト由来の腎細胞で評価を行う場合、種差の問題が解消されることに加え、多くの化合物についてのデータをよりスピーディに、研究の初期段階から取得できるため、創薬の時間短縮やコスト削減も期待できます。しかしながら、創薬研究におけるニーズを満たすヒト腎細胞はこれまで存在しませんでした。
■各研究機関の役割
日機装株式会社:これまで培ってきた細胞培養技術を基に、腎細胞の機能を発現する培養条件および製造方法を確立
日本ベーリンガーインゲルハイム株式会社:世界をリードする薬物トランスポーターの知見と蛋白質定量の技術を基に、創薬研究への実装化に貢献
金沢大学医薬保健研究域薬学系 玉井郁巳教授らの研究グループ:当該細胞を用いた、薬物の安全性および薬物動態に関する評価手法を確立
■研究成果の概要
従来のヒト腎細胞(HK-2細胞や初代近位尿細管上皮細胞)は、通常の培養環境では、生体の腎臓と比較して腎臓特有の機能の多くが失われていることが知られています(Jenkinson et al., Eur J Physiol, 2012)。そのため、創薬研究の現場では、多くの場合、動物実験により腎臓の評価を行ってきました。本研究では、ヒト近位尿細管上皮細胞(RPTEC)を平面培養では発現しないOAT1(有機アニオントランスポーター1)の遺伝子を指標として培養条件を検討し、RPTECの腎臓の機能改善を試みました。スフェロイド(以下、3D-RPTEC)を作製し、一定の条件下で3次元培養すると、OAT1遺伝子発現が培養日数とともに上昇し、ヒト腎皮質のmRNA発現量と同程度に改善されました(図1)。本細胞については、マイクロアレイによる網羅的遺伝子発現解析およびプロテオミクスによる網羅的蛋白質発現解析を実施しました。その結果、OAT1以外の規制当局が評価を求めるSLC トランスポーターについても、平面培養と比較して3次元培養することで改善が見られ、培養32日後でもその発現が維持されていました(図2)。
また、異なる3つのドナー由来のRPTECを3次元培養した場合の mRNA発現解析において、約17000 遺伝子のうち87%がCV% 50%のばらつきしか示さなかったことから、3D-RPTECはドナー差が少なく利用しやすい細胞であることが明らかになりました。薬物評価例として、細胞内ATP量(生存率)を指標としたin vitro毒性試験を実施しました。その結果、薬物トランスポーターに起因した腎毒性を示すCisplatinとAdefovirが、濃度依存的に細胞内ATP量を減少させ、その減少は、それぞれOCT(有機カチオントランスポーター)の阻害剤であるCimetidine、OAT(有機アニオントランスポーター)の阻害剤であるProbenecidで抑制されました(図3)。このことから、3D-RPTECは医薬品開発における薬物動態や毒性評価において、簡便でスループットの高いin vitro実験系であることが示されました。
要約すると、RPTECでスフェロイドを作製し、一定の条件下で3次元培養することで腎臓の主要機能の1つである薬物トランスポーターがヒト腎臓と同程度に発現し、またその発現が28日以上と長期間維持されることが明らかになりました(特許第6995112号)。また、3D-RPTECを用いて薬物トランスポーターに起因した腎毒性を観察することが示されました。さらに、薬物トランスポーターだけでなく、プロテオミクスで検出した約4800のタンパク質の90%が、ヒト腎臓と同程度の発現を示していることから、3D-RPTECは、医薬品開発における薬物動態や毒性評価において、簡便でスループットの高いin vitro実験系であることが示されました。また創薬研究だけでなく、腎臓に関連する様々な研究に使用可能なヒト腎細胞であると期待されます。
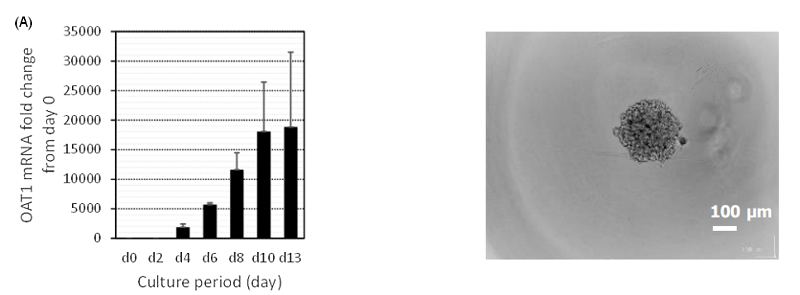
図1. 3D-RPTECの培養日数とOAT1遺伝子発現
3D-RPTEC(左図)は培養日数とともにOAT1の遺伝子発現量が増加し、培養10日目以降で最大となった。
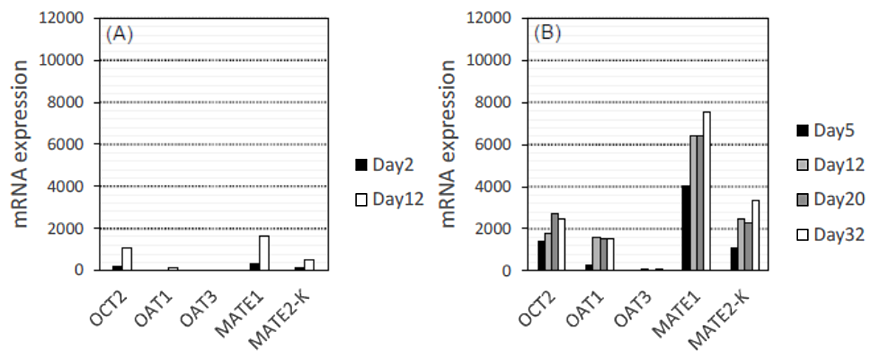
図2. 3D-RPTECのマイクロアレイ解析
従来の平面培養におけるRPTECの遺伝子質発現量(A)と3D-RPTECにおける遺伝子発現量(B)を示す。従来の平面培養と比較して3D-RPTECでは薬物トランスポーターの発現量が改善され、培養12日目から32日目まで発現が維持されることが確認できた。
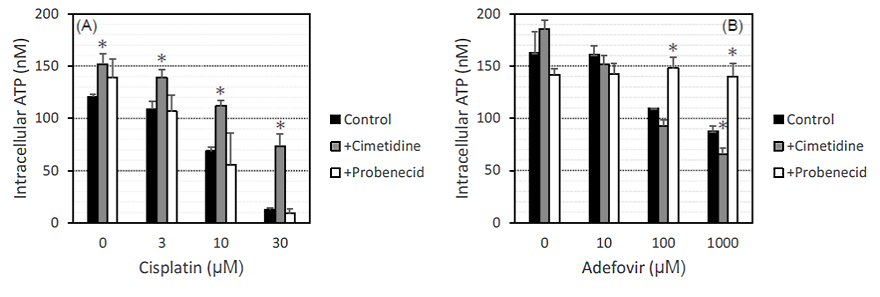
図3. 3D-RPTECを用いたin vitro毒性試験
3D-RPTECにCisplatinを曝露した際の細胞内ATP量(A)と、Adefovirを曝露した際の細胞内ATP量(B)を示す。OCTおよびOATの阻害剤を用いた結果、3D-RPTECは薬物トランスポーターに起因した毒性を検出できることが確認できた。
■論文掲載
雑誌名:Drug Metabolism and Disposition
論文名:Improvement of protein expression profile in three-dimensional renal proximal tubular epithelial cell spheroids selected based on OAT1 gene expression: a potential in vitro tool for evaluating human renal proximal tubular toxicity and drug disposition
著書名:Naoki Ishiguro1, Etsushi Takahashi2, Hiroshi Arakawa3, Asami Saito1, Fumihiko Kitagawa2, Masayuki Kondo2, Gaku Morinaga1, Masahito Takatani1, Ryo Takahashi1, Takashi Kudo1, Shin-ichi Mae4, Moeno Kadoguchi3, Daichi Higuchi3, Yuya Nakazono3, Ikumi Tamai3, Kenji Osafune4, Yoichi Jimbo2
1: Pharmacokinetics and Non-Clinical Safety Department, Nippon Boehringer Ingelheim Co., Ltd., Kobe, Japan
2: R&D Department, Industrial Division, Nikkiso Co., Ltd., Kanazawa, Japan
3: Faculty of Pharmaceutical Sciences, Institute of Medical, Pharmaceutical and Health Sciences, Kanazawa University; Kanazawa, Japan
4: Center for iPS Cell Research and Application (CiRA), Kyoto University, Kyoto, Japan
掲載日時:2023年6月29日
■今後の展開
本研究成果により、日機装株式会社は創薬研究用ヒト腎細胞『3D-RPTEC®(スリーディーアールピーテック)』を製品化し、2023年7月から正式販売を開始しています。
今後、腎臓評価を予測するツールとして3D-RPTECを多くの研究現場で使っていただくことで、ヒト腎細胞を用いた細胞実験の標準化を目指しています。
※「3D-RPTEC」は日機装株式会社の登録商標です。
<日機装 会社概要>
| 会社名: | 日機装株式会社 |
| 本社所在地: | 東京都渋谷区恵比寿4丁目20番3号恵比寿ガーデンプレイスタワー22階 |
| 創業: | 1953年12月26日 |
| 代表者: | 代表取締役社長 甲斐 敏彦 |
| 事業内容: | 産業用特殊ポンプ・システム、医療機器、航空機部品等の製造・販売 |
| URL: | https://www.nikkiso.co.jp/ |
<日本ベーリンガーインゲルハイム 会社概要>
| 会社名: | 日本ベーリンガーインゲルハイム株式会社 |
| 本社所在地: | 東京都品川区大崎2-1-1 |
| 設立: | 1961年6月30日 |
| 代表者: | 代表取締役会長 兼 社長 シャシャンク・デシュパンデ |
| 事業内容: | 医薬品の研究開発、輸入、製造、販売 |
| URL: | https://www.boehringer-ingelheim.com/jp/ |
<金沢大学 概要>
| 法人名: | 金沢大学 |
| 所在地: | 石川県金沢市角間町 |
| 設立: | 1949年5月31日 |
| URL: | https://www.kanazawa-u.ac.jp |

